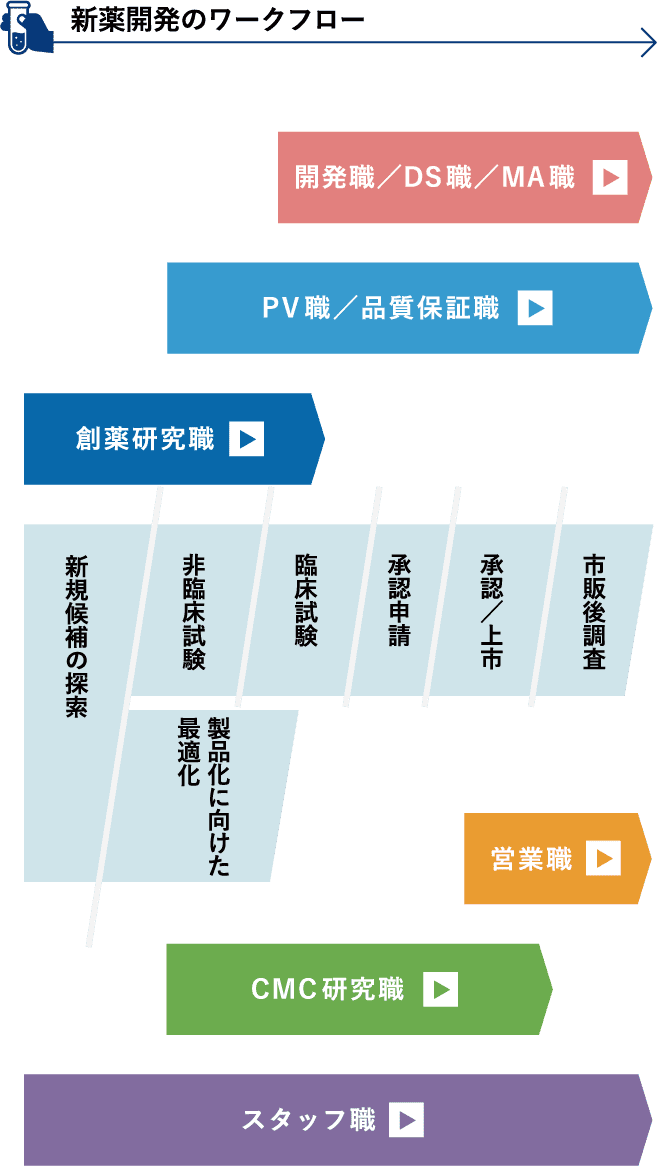
患者さんやそのご家族へ“希望ある選択肢”をお届けするために、
それぞれの部門が連携を図りながら創薬・育薬に挑戦しています。
創薬研究職
メディシナルケミストリー
創薬化学とも呼ばれ、リード化合物の創製に向けた探索合成研究、および開発候補化合物を取得するためのリード化合物の最適化合成研究を行います。その過程では、リード化合物の作用機序を明らかにすることや、薬効向上や物性改善のための化合物デザインなどに至るまで幅広い領域をカバーするため、有機化学をはじめ、計算化学、ドラッグデザイン、化学工学など化合物に関する知識や実験技術を駆使します。
近年は、低分子医薬品だけでなく核酸医薬品やペプチド医薬品、異なるタンパク質間の相互作用を制御する医薬品の創製に向けた探索および最適化研究などにも取り組んでいます。
生物(薬理/スクリーニング)研究
薬理学、生化学、分子生物学、細胞生物学、バイオインフォマティクス等さまざまな知識を活用しながら、創薬ターゲットの発掘、新薬候補化合物の有効性や有用性の評価を行う研究です。
遺伝子組換え技術、初代培養技術、iPS技術などを活用して、細胞を用いたin vitro生物活性試験系を構築し、化合物評価に取り組んでいます。また、この構築した試験系を大規模スクリーニング(HTS)へ適用することで、新規化合物の探索と評価を行っています。さらに、高次評価系として病態モデル動物を用いたin vivo生物活性試験系を構築し、有望な化合物の薬効評価も担っています。
その他、大量の生物学的データ・ICTを用いた疾患解析、創薬ターゲット探索及び薬剤作用予測、薬物の物性および薬物動態特性の解析、更にはその制御に基づく薬物送達技術の構築なども手がけています。
バイオロジクス
生化学、分子生物学、細胞工学、遺伝子工学等の知識を活用しながら、遺伝子やタンパク質、細胞などの生物材料や機能を用いて製造される医薬品(バイオロジクス)について、創薬標的の探索研究、生物学的評価、原薬プロセス開発・初期CMC構築(細胞構築、培養、精製、スケールアップ研究)、試験法(分析)技術開発を行っています。国内でいち早くバイオロジクスを手がけた実績を活かしつつ、抗体医薬、遺伝子治療、ワクチンなどの創薬研究に取り組んでいます。
薬物動態研究
投薬した候補化合物の体内での吸収、分布、代謝、排泄に関する特性を調べます。薬物動態の特性は有効性、安全性を大きく左右するため、非臨床段階での研究もきわめて重要です。特に、開発段階の前、候補化合物がヒトの体内でどのような挙動をするかをあらかじめ予測するための研究に力を入れています。
具体的な取り組みとしては、マウスなどを用いた動物実験によるin vivo試験をはじめ、ヒトもしくは実験動物などの組織や細胞といった生体由来試料を用いたin vitro試験、さらにはin silicoとしてコンピュータを活用したモデリングおよびシミュレーションなども手がけています。
安全性研究
探索合成研究を経た後、培養細胞や動物実験などヒト以外を対象にした非臨床試験を通じて、開発候補化合物の安全性に関する研究を推進しています。一般毒性や細胞毒性、遺伝毒性、発がん性など多岐にわたる観点から安全性を評価していきます。これによって、ヒトにおける副作用などの有害事象の発現リスクを予測することが可能となります。
毒性学や病理学、実験動物学、分子生物学、細胞生物学など専門性の高い知見を活かした取り組みを通じて、候補化合物の絞り込みや臨床試験(治験)を行う上で欠かせないデータを提供しています。患者さんに安心して処方できる医薬品を開発する上で欠かせない研究の一つです。
開発職/DS職/MA職
開発
非臨床試験で有効性や安全性が確認された開発候補化合物について、ヒトでの臨床試験(治験)を実施して、そのデータに基づき当局へ承認申請を行い、医薬品として世の中に送り出すお仕事です。具体的な業務内容としては、治験の計画立案・医療機関との契約手続き・治験のモニタリング・総括報告書の作成・承認申請資料作成等が挙げられます。それぞれの過程では、規制当局・医師・海外協業会社ともサイエンスベースで議論します。これらの業務は社内の開発チームで実施しますが、医薬品開発業務受託機関(CRO)など社外と連携することも多いため、より早く患者さんにお届けするためにはプロジェクトマネジメントも重要となります。
データサイエンス(DS)
臨床試験(治験)によって得られたデータを管理・解析するお仕事です。データの品質や信頼性を確保する上で欠かせない役割を担います。具体的な業務内容としては、統計解析計画の立案・症例報告書の設計・医療機関から収集したデータの品質チェック・データ解析などが挙げられます。治験の計画、実施、評価に至るまで統計学の専門的な観点から助言を行い、信頼性の高い治験結果が得られるように支援していきます。また、世界標準仕様のデータ作成および解析結果の作成はグローバルに行っており、全世界の試験を日本のチームを中心に管理しています。
メディカルアフェアーズ(MA)
メディカルアフェアーズ(MA)/メディカルサイエンスリエゾン(MSL)とは、製品の販売活動を担当する職種から独立し、医学的・科学的に高度な専門性、学術知識を持ち、社外・社内において医学的・科学的な面から製品の適正使用、製品価値の至適化等を推進する職種です。 特に、社外での医学専門家、研究者等との医学的・科学的な議論や学会活動等を通じて、アンメットメディカルニーズの解決に寄与することも担っています。
PV職/品質保証職
ファーマコビジランス
医薬品は、病気に対して効果をもたらす一方で、副作用のリスクを伴います。そのため各製薬会社は、その薬をどのように使えば患者さんへのベネフィットを最大化し、リスクを最小限にできるかについて、日々情報を収集、分析、発信しています。 ファーマコビジランスは、「医薬品の安全性監視」と訳されます。これは、どの国で起こった副作用であっても、その情報をグローバルに共有し、各々の国での安全管理に役立てようとする考え方です。現在、田辺三菱製薬では、特徴ある医薬品を扱っており、医療に広く役立てて頂いています。ファーマコビジランス職では、当社の医薬品に関して世界から集めた多くのデータを科学的に分析・評価し、ベネフィット・リスクに関する情報をグローバルに発信しています。
品質保証
医薬品は、最終製品の製品品質のみならず、その製造プロセスも適切でなければなりません。また、製品は販売されている各国のレギュレーションに適合した品質でなければなりません。さらには、開発ステージにおける治験薬の品質も製薬企業は保証しなければなりません。このように、グローバルなフィールド・幅広いステージ・各製造工程が、医薬品の品質保証職が活躍する場となります。そのため、医薬品の品質保証職は“医薬品の特性や各製造プロセスを理解するためのサイエンス” 、“海外を含めた共同開発企業や製造所と円滑に意見交換して推進するコミュニケーション力”を日々高める努力が必要です。そして何より、患者さんに安心・安全な医薬品を届ける“最後の砦” としての使命感を持って仕事をすることが求められています。
CMC研究職
プロセス研究
CMC(Chemistry、Manufacturing and Control)が原薬・製剤の「化学」「製造」「品質管理」の情報を扱う業務である中で、プロセス研究は開発候補品の有効成分である原薬(低分子、中分子(核酸等)及び高分子(抗体、タンパク質等)等)について、品質や安全性、コストを考慮しつつ工業化が可能な製造プロセスを設計し、その製造法を最適化する研究です。前臨床及び臨床試験用の治験原薬の製造・供給のための製法検討や、商業生産を指向したスケールアップ検討、種々の生産場所への技術移管などに取り組んでいます。一方で、プロセス研究に関する新規技術開発・導入も推進し、より効率的な製造法確立のために日々検討を行っています。
製剤研究
新規医薬品の開発において薬理活性のある化合物(有効成分)のポテンシャルを最大限に引き出すべく製剤機能を付与し、優れた品質で、かつ患者さんの使用しやすい最適な製品形態とする研究を行っています。臨床試験(治験)段階での治験薬の製造および供給や、商業生産を指向して、新規製剤の処方設計からプロセス設計、包装設計、工業化研究を開発ステージに応じて実施しています。より品質の高い製剤を効率よく生産するための新規製造法の開発をはじめ、製品価値を向上させるための新剤形および新規包装形態の開発、革新的な技術取得のための製剤、包装に関する基盤研究にも取り組んでいます。
物性分析研究
低分子医薬品から核酸、抗体等のバイオ医薬品に至る広範囲な開発候補品の物性分析研究を行っています。開発候補品の品質を評価するため、各化合物に適した試験方法を開発し、化合物の構造解析及び物理化学的、生化学的、微生物学的評価を実施、製剤については製剤特性、生物薬剤学的評価なども行います。また、開発した試験方法を生産工場に技術移管しています。加えて、分析に関する新規基盤技術開発にも取り組んでいます。
研究開発の初期段階から市販後に至るまで医薬品のライフサイクル全般に関わることで、より良い品質の医薬品開発をめざしています。
営業職
MR職
MR(Medical Representative)とは「医薬情報担当者」の意味で、自社医薬品の適正使用情報の提供と普及を図ることが主な仕事です。具体的には、医師や薬剤師など医療関係者に対して、医薬品の品質や安全性、有効性に関する詳細な情報をタイムリーに提供します。それとともに、使用された医薬品が想定された効能を発揮できているか、もしくは発売前に不明であった副作用が生じていないかなどの情報を収集することも重要な仕事です。MRを通じて広く収集された情報はさまざまな角度から分析され、新たな情報として医療関係者に伝達されます。
こうした取り組みを通じて、患者さんの治療に貢献することを使命としています。
スタッフ職
スタッフ職
医薬品を患者さんにお届けするという社会的な使命を果たす上で、その活動を支える業務をスタッフ職が担います。この中には、経営企画、製品戦略、総務、経理・財務、人事、広報、法務・知財、海外事業、BD(ビジネスディベロップメント)など多岐にわたる業務があり、それぞれの分野のエキスパートが「自らの仕事を通じて医療に貢献できることは何か」という意識を常にもって、日々業務に取り組んでいます。